miércoles, 21 de marzo de 2018
semana 8
ACTIVIDAD INICIAL: Con los numeros
3 4 5
6 7 8
9 10 11
Organizarlos en la gráfica de tal forma que en todas sus diagonales de 21.
-Modelo actual del átomo:
-Naturaleza de la luz ---> onda- E
---> particulas---> materia---> Cuantos o fotones
-Mecanica cuantica---- micro
fue propuesto en 1954 por 4 cientificos ganadores del premio nobel
-E. Sommerfield
-L. Pauling
-Schrodinger
-Heisemberg
En el modelo actual se diferencian dos partes fundamentales:
-Nucleo: En el se encuentra los protones descubiertos por Rutherford y los neutrones (n) descubiertos por Chadwick.
-Corteza: esta constituida por los niveles de energia que forman el numero cuadratico principal (n) ---> niveles de energia se nombran de la letra K - L - M - N - O - P - Q
Con los numeros del 1 - 2 - 3 - 4 - 5 - 6 - 7
El segundo numero cuántico se denomina con la letra L minúscula y determina la forma del orbital
-Orbital: es el espacio volumetrico donde hay mayor probabilidad de encontrar un electrón en un numero determinado.

El 3 numero cuantico magnetico (me) define la orientacion que puedan tomar el orbital.
s - 1orb
p - 3orb
d - 5orb
f - 7 orb
El cuarto nivel se dedomina spin (sm) el electron presenta dos giros sobre u propio eje

El electron presenta dos maners de giro, a sentido del reloj presenta el valor de 1/2 y si gira al contrario del reloj toma el valor de -1/2
-Distribucion electronica

3 4 5
6 7 8
9 10 11
Organizarlos en la gráfica de tal forma que en todas sus diagonales de 21.
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
-Modelo actual del átomo:
-Naturaleza de la luz ---> onda- E
---> particulas---> materia---> Cuantos o fotones
-Mecanica cuantica---- micro
fue propuesto en 1954 por 4 cientificos ganadores del premio nobel
-E. Sommerfield
-L. Pauling
-Schrodinger
-Heisemberg
En el modelo actual se diferencian dos partes fundamentales:
-Nucleo: En el se encuentra los protones descubiertos por Rutherford y los neutrones (n) descubiertos por Chadwick.
-Corteza: esta constituida por los niveles de energia que forman el numero cuadratico principal (n) ---> niveles de energia se nombran de la letra K - L - M - N - O - P - Q
Con los numeros del 1 - 2 - 3 - 4 - 5 - 6 - 7
El segundo numero cuántico se denomina con la letra L minúscula y determina la forma del orbital
-Orbital: es el espacio volumetrico donde hay mayor probabilidad de encontrar un electrón en un numero determinado.

El 3 numero cuantico magnetico (me) define la orientacion que puedan tomar el orbital.
s - 1orb
p - 3orb
d - 5orb
f - 7 orb
El cuarto nivel se dedomina spin (sm) el electron presenta dos giros sobre u propio eje
El electron presenta dos maners de giro, a sentido del reloj presenta el valor de 1/2 y si gira al contrario del reloj toma el valor de -1/2
-Distribucion electronica

semana 6
Implemento del laboratorio.
Tubos de ensayo
Estos recipientes sirven para hacer experimentos o ensayos, los hay en varias medidas y aunque generalmente son de vidrio también los hay de plástico.
Gradilla
Utensilio que sirve para colocar tubos de ensayo. Este utensilio facilita el manejo de los tubos de ensayo.
Refrigerante de rosario
Es un refrigerante que también recibe el nombre de: Refrigerante de Allin. Es un tubo de vidrio que presenta en cada extremo dos vástagos dispuestos en forma alterna. En la parte interna presenta otro tubo que se continúa al exterior, terminando en un pico gotero. Su nombre se debe al tubo interno que presenta. Se utiliza como condensador en destilaciones.
Refrigerante de serpentín
Es un refrigerante que también recibe el nombre de: Refrigerante de Graham. Su nombre se debe a la característica de su tubo interno en forma de serpentín. Se utiliza para condensar líquidos.
Refrigerante recto
Es un refrigerante que también recibe el nombre de: Refrigerante de Liebing. Su nombre se debe a que su tubo interno es recto y al igual que los otros dos refrigerantes se utiliza como condensador.
Cristalizador
Este utensilio permite cristalizar sustancias.
Matraz de reaccion
Es un recipiente que permite contener sustancias.
Matraz de destilación
Es un recipiente que se utiliza para contener sustancias es una variación del matraz balón.
Balones
Un balón de destilación es parte del llamado material de vidrio. Es un frasco de vidrio, de cuello largo y cuerpo esférico.
Balon con base
Es un recipiente que se utiliza para contener sustancias es una variación del matraz balón.
Vidrio de reloj
Es un utensilio que permite contener sustancias corrosivas.
Pizeta
También llamada frasco lavador o matraz de lavado la pizeta es un frasco cilíndrico de plástico con pico largo, que se utiliza en el laboratorio de química o biología, para contener algún solvente, por lo general agua destilada o desmineralizada, aunque también solventes orgánicos como etanol, metanol, hexano, etc.
Mortero y pilón
Son utensilios hechos de diferentes materiales como: porcelana, vidrio o ágata, los morteros de vidrio y de porcelana se utilizan para triturar materiales de poca dureza y los de ágata para materiales que tienen mayor dureza.
Tubo en U
el tubo en U funciona como deposito a través del cual se transmite la presión.
Soporte Universal
Es un utensilio de hierro que permite sostener varios recipientes.
Varilla
Están hechos de varilla de vidrio y se utilizan para agitar o mover sustancias, es decir, facilitan la homogenización.
Matraz Erlenmeyer
Es un recipiente que permite contener sustancias o calentarlas.
Materiales
-Soporte universal
-Mechero de alcohol
-Pinzas
-beaker (vaso de precipitacion)
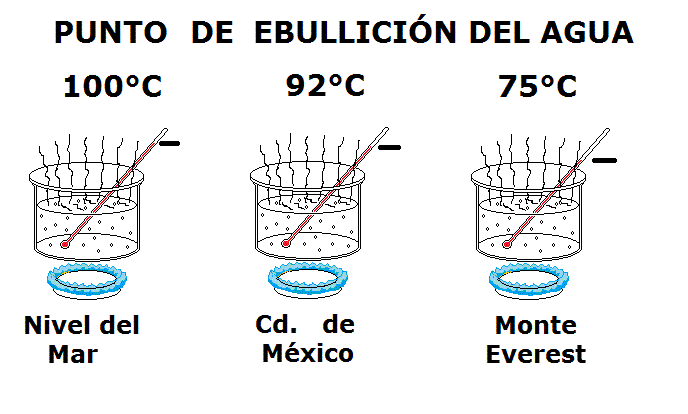
Temperatura inicial 20° --->40°--->93° Punto de ebullicion
semana 5
Semana numero 5
ACTIVIDAD INICIAL: La suma de los números suma 20 y la multiplicación entre si es 99.
9 y 11 = 9 + 11 = 20
9 * 11 = 99
En la clase del día 13/02/2018 se rea.lizo un taller e parejas en que el consistía que en los equipos se repartiera el trabajo así terminando y agilizando todo, este consistía que en cada punto se escogiese una parte para realizar y solucionar y el tema asignado era de peso de un átomo y molécula.
ACTIVIDAD INICIAL: ¿Que cifra completa el cuadro?
Principales métodos de separación de mezclas

9 y 11 = 9 + 11 = 20
9 * 11 = 99
En la clase del día 13/02/2018 se rea.lizo un taller e parejas en que el consistía que en los equipos se repartiera el trabajo así terminando y agilizando todo, este consistía que en cada punto se escogiese una parte para realizar y solucionar y el tema asignado era de peso de un átomo y molécula.
ACTIVIDAD INICIAL: ¿Que cifra completa el cuadro?
5
|
4
|
3
|
9
|
5
|
7
|
3
|
9
|
3
|
2
|
Principales métodos de separación de mezclas
Existen varios métodos de separación de mezclas, que como ya dijimos, se usarán de acuerdo a las características de los componentes de la mezcla. Estas son algunos de los principales de separación de mezclas:
Separación de mezclas por decantación: Por este método, se desaloja un líquido que está mezclado con un sólido. También se usa para separar dos líquidos de diferentes densidades, ya que uno flotará sobre del otro.
Ejemplo: Cuando mezclamos agua con aceite y lo dejamos reposar, el aceite, por ser menos denso, se acumulará sobre el agua; si inclinamos el vaso que los contiene, podemos separar el aceite que comenzará a fluir al recipiente donde lo estemos recolectando.
2.Separación de mezclas por filtración: Cuando tenemos en un líquido una sustancia que no se disuelve, podemos filtrarla. El filtrado consiste en pasar a través de un cuerpo poroso (tela, papel y ciertas piedras, el líquido con las partículas que están en el líquido. Las partículas sólidas serán retenidas por el filtro, mientras que el agua pasará al otro lado del filtro.
Ejemplo: El ejemplo más común de esto, son las cafeteras. Una vez que ha hervido el agua con los granos de café, pasa por un filtro que deja pasar la infusión, y retiene el café molido.
Separación de mezclas por evaporación: Cuándo una sustancia se disuelve en un líquido y no puede ser filtrado, la sustancia disuelta se puede recuperar haciendo hervir el líquido hasta que se evapore, quedando en el fondo del recipiente la sustancia con que se había combinado.
Ejemplo, este es el método que se usa en las salinas, donde el agua de mar es extendida en evaporadores donde le dan los rayos del sol; una vez que el agua se ha evaporado, queda en el evaporador la sal que estaba disuelta.
semana 4
La temperatura
es una propiedad de la materia que está relacionada con la sensación de calor o frío que se siente en contacto con ella cuando tocamos un cuerpo el mayor o menor grado de agitación de las moléculas reaccionando con la cantidad de energía cinética de las mismas.
es una propiedad de la materia que está relacionada con la sensación de calor o frío que se siente en contacto con ella cuando tocamos un cuerpo el mayor o menor grado de agitación de las moléculas reaccionando con la cantidad de energía cinética de las mismas.
Nombre
|
Símbolo
|
Temperatura de referencia
|
equivalencia
|
Escala Celsius
|
°C
|
Punto de congelación (0°C) y ebullición del agua (100 °C).
| |
Escala Fahrenheit
|
°F
|
Punto de congelación de una mezcla anticongelante de agua y sal y temperatura del cuerpo humano
| |
Escala kelvin
|
°K
|
Cero absoluto (Temperatura más baja posible) y punto triple del agua (H2O)
|
K = °C + 273
|
Hg ------> Metal------>Calor----->Dilatan
omsnm------> frio----->se contrae
(FORMA Y VOLUMEN DEFINIDOS)
Gaseoso----->forma indefinida------>depende del recipiente
Volumen----->depende del recipiente
Unidades Químicas
-Unidad de masa atomica (u.m.a) = C = 1 uma
-Atomo gramo: es el peso atomico expresado en gramos
C = 12 uma ---> 12g C----> 1 atomo gramos
- Mol = Asociada con la docena (6.023 *10^23 particulas)
602.300.000.000.000.000.000.000 = 12gC = 1 molecula
H2O = 18g/molecula
ACTIVIDAD INICIAL: reflexion sobre "Dios nos ama" resaltando y mostrando todo aquello que Dios nos ha dado y sigue dando siendo lo bonito de la vida.
Unidades quimicas
U.M.A: es la unidad quimica de referencia para indicar el peso masa de los atomos se tomo al C (carbono) como referencia y se le asigna un valor de C = 12 uma
Mol ó mole: Es una cantidad de particulas iguales al numero de avogrado = 6.023*10^23
Atomo-gramo: es el peso o masa atomico expresado en gramos
C= 12 uma---> 12g = 1at - g = 1mol = 6.023*10^23 particulas
Masa molar o peso molecular: Se obtiene al sumar las masas atomicas de los atomos que hay en un compuesto.
H2 = 1uma * 2 = 2uma ---> 2g/mol
H2O = H = 1uma * 2 = 2uma
O = 16uma * 1 = 16uma
18uma ---> 18g/mol ---> 6.023*10^23
K = 39uma
Cl = 35.5uma
O = 16uma
P = 31uma
H = 1 uma
Al = 27uma
Ca = 40 uma
S = 32uma
Mn = 55.8uma
KCLO3 = K = 39uma * 1 = 39uma
Cl = 35.5uma * 1= 35.5uma
O = 16uma * 3 = 48uma
H3PO4 = H = 3 * 1uma = 3uma
P = 1 * 31uma = 31uma
O = 4 *16uma = 64uma
98uma ---> 98 g/mol
Al(OH)3 = Al = 1 * 27uma = 27uma
O = 3 * 16uma = 48uma
H = 3 * 1uma = 3uma
78uma ---> 78g/mol
Propiedades Generales:
Son las propiedades que presenta todo cuerpo material sin excepción y al margen de su estado físico, así tenemos:
- Masa: Es la cantidad de materia contenida en un volumen cualquiera, la masa de un cuerpo es la misma en cualquier parte de la Tierra o en otro planeta.
- Volumen: Un cuerpo ocupa un lugar en el espacio
- Peso: Es la acción de la gravedad de la Tierra sobre los cuerpos. En los lugares donde la fuerza de gravedad es menor, por ejemplo, en una montaña o en la Luna, el peso de los cuerpos disminuye.
- Divisibilidad: Es la propiedad que tiene cualquier cuerpo de poder dividirse en pedazos más pequeños, hasta llegar a las moléculas y los átomos.
- Porosidad: Como los cuerpos están formados por partículas diminutas, éstas dejan entre sí espacios vacíos llamados poros.
- La inercia: Es una propiedad por la que todos los cuerpos tienden a mantenerse en su estado de reposo o movimiento.
- La impenetrabilidad: Es la imposibilidad de que dos cuerpos distintos ocupen el mismo espacio simultáneamente.
- La movilidad: Es la capacidad que tiene un cuerpo de cambiar su posición como consecuencia de su interacción con otros.
- Elasticidad: Propiedad que tienen los cuerpos de cambiar su forma cuando se les aplica una fuerza adecuada y de recobrar la forma original cuando se suspende la acción de la fuerza. La elasticidad tiene un límite, si se sobrepasa el cuerpo sufre una deformación permanente o se rompe. Hay cuerpos especiales en los cuales se nota esta propiedad, como en una liga, en la hoja de un cuchillo; en otros, la elasticidad se manifiesta poco, como en el vidrio o en la porcelana.
Propiedades especificas:
Son las propiedades peculiares que caracterizan a cada sustancia, permiten su diferenciación con otra y su identificación.
Entre estas propiedades tenemos: densidad, punto de ebullición, punto de fusión, índice de refracción de luz, dureza, tenacidad, ductibilidad, maleabilidad, solubilidad, reactividad, actividad óptica, energía de ionización, electronegatividad, acidez, basicidad, calor latente de fusión, calor latente de evaporización, etc.
Las propiedades especificas pueden ser químicas o físicas dependiendo si se manifiestan con o sin alteración en su composición interna o molecular.
1. Propiedades Físicas: Son aquellas propiedades que impresionan nuestros sentidos sin alterar su composición interna o molecular.
Ejemplos: densidad, estado físico (solido, liquido, gaseoso), propiedades organolépticas (color, olor, sabor), temperatura de ebullición, punto de fusion, solubilidad, dureza, conductividad eléctrica, conductividad calorífica, calor latente de fusión, etc.
A su vez las propiedades físicas pueden ser extensivas o intensivas.
- Propiedades Extensivas: el valor medido de estas propiedades depende de la masa. Por ejemplo: inercia, peso, área, volumen, presión de gas, calor ganado y perdido, etc.
- Propiedades Intensivas: el valor medido de estas propiedades no depende de la masa. Por ejemplo: densidad, temperatura de ebullición, color, olor, sabor, calor latente de fusión, reactividad, energía de ionización, electronegatividad, molécula gramo, átomo gramo, equivalente gramo, etc.
2. Propiedades Químicas: son aquellas propiedades que se manifiestan al alterar su estructura interna o molecular, cuando interactúan con otras sustancias.
Ejemplos: El Fe se oxida a temperatura ambiental y el Oro no se oxida; el CH4 es combustible y el CCl4 no es combustible; el Sodio reacciona violentamente con el agua fria para formar Hidróxido de Sodio y el Calcio reacciona muy lentamente con el agua para formar Hidróxido de Calcio; el alcohol es inflamable y el H2O no lo es; el acido sulfúrico quema la piel y el acido nítrico no, etc.
Resumiendo, las propiedades químicas de la materia son:
- Reactividad Química
- Combustión
- Oxidación
- Reducción
Punto de ebullición: proceso que se produce al cambio de estado de una materia que pasa de líquido a gaseoso. Asimismo, se refiere a la temperatura que provoca que la presión del vapor de un líquido iguale la presión del vapor por medio de la ebullición.
Punto de fusión: Hace referencia a la temperatura en la cual la materia cambia de estado cuando hablamos de un solido, pasando a estado liquido tras fundirse. el punto de fusión de un solido cristalino es la temperatura del cambio del estado solido al liquido, cuando se encuentra a la presión de 1 atmósfera.
Viscosidad: Es una característica de los fluidos en movimiento, que muestra una tendencia de aposición hacia su flujo ante la aplicación de una fuerza. cuanta mas resistencia aponen los líquidos a fluir mas viscosidad poseen.
Suscribirse a:
Comentarios (Atom)